VARIAN RT REPORT
2018年7月号
ここまでできるがん放射線治療シリーズ No.6 特別企画:SBRT治療実績世界トップクラスの病院に聞く臨床アップデート
3)前立腺がんに対するRapidArcを用いた体幹部定位放射線治療
鶴貝雄一郎/武田 篤也/奥 洋平(大船中央病院放射線治療センター)
はじめに
前立腺がんに対する体幹部定位放射線治療(stereotactic body radiation therapy:SBRT)は,2003年頃に北米で低~中リスク患者を対象に開始された。2014年頃からは経過観察期間中央値6~9年の報告1),2)が散見されるようになり,既存の治療法と同等の治療成績と有害事象が示されている。最近では高リスク前立腺がんにも適応が拡大されつつあるが,長期的な治療成績は十分とは言えない。その状況で,本邦では2016年春に保険収載された。
われわれは,保険収載と同時に前立腺がんに対してSBRTを開始した。照射方針の決定においては,複数の治療法それぞれの得失や臨床経験を率直に説明し,患者と相談しながら治療方針を決定するshared decision makingを実践している。その結果,2016年4月〜2018年4月までの前立腺がん放射線治療患者240例中133例(55%)がSBRTを選択した。SBRT開始後,家族の介護や仕事などで長期間の通院が困難なために,今までであればホルモン療法単独や手術としていた患者に対して,他院の泌尿器科医がSBRTを勧めて当院を受診する例も増えている。言い換えれば,SBRTは,より多くの患者に高精度放射線治療を提供する機会の掘り起こしにもなっていると実感している。
前立腺がんにSBRTを行う際の注意点
前立腺は直腸の容量や肛門括約筋の緊張具合いの変化によって,比較的大きく変位する。一方で,SBRTでは計画標的体積(PTV)マージンが3〜5mmと小さく設定されるため,照射時間中の前立腺の変位に細やかに対応することが求められる。われわれはcone beam CT(CBCT)で位置補正を速やかに行うとともに,直腸の状態を適宜調整して対応している(図1)。さらに,緊張しやすい患者や仰臥位になるとしばらく腰痛が出現する患者の場合は,体の緊張や腰痛がなくなるまでCBCT撮影開始を待つなどの工夫をしている。SBRT開始当初の29例に対する,計283CBCTにおける照射前後の前立腺の背側への変位量を示す(図2)。その結果,初回CBCT撮影開始から8分以内であれば,変位量の95パーセンタイルが3mm以内に収まっていた。
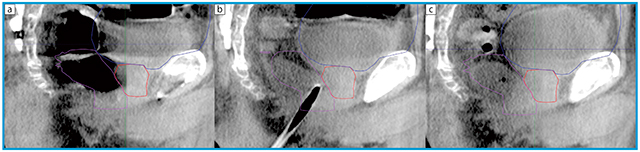
図1 直腸内ガス貯留例への対応(CBCT矢状断)
初回CBCTにて,ガス貯留のために直腸(ー)が著明に拡張しており,治療計画時の前立腺(ー)にまでかかっていた(a)。そこで,ネラトンチューブでガスを抜き(b),その後は治療計画時の位置関係を再現した状況で照射を行った(c)。治療計画時に比べて膀胱(ー)の容量が少ないが,膀胱容量の多寡によって前立腺の圧排や傾きはほとんど変わらない印象を持っている。
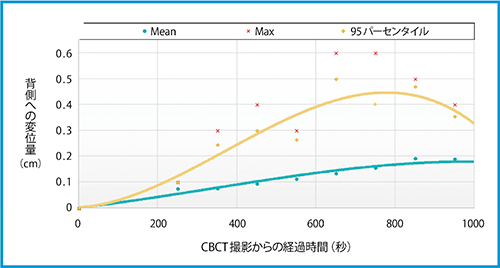
図2 前立腺の背側への変位量と経過時間の関係
各arc前後の変位量を合算し,仮想的に初回arc前から2arc目照射後までカウチを移動しなかった場合の変位量を算出した。初回CBCTから480秒(8分)以内であれば,変位量の95パーセンタイル近似曲線がPTV設定マージンの3mm以内であることがわかる。
線量分割とSIB
SBRTでも線量増加の流れにある。欧米において,当初32.5〜33.5Gy/5回で開始され,現在は36.25Gy/5回が主流となっている。最近では,高リスク前立腺がんにも適応が拡大されつつあり,40〜50Gy/5回3),4)へのさらなる線量増加も試みられている。線量が増加するにつれて毒性は増える傾向にあり,がんの制御と晩期毒性のトレードオフが模索されている。その状況の中で,MRIで描出可能な病変にだけ処方線量より高い線量を投与するsimultaneous integrated boost(SIB)の報告5),6)も散見されるようになっている。われわれは,前立腺がんの悪性度や腫瘍の存在部位に応じて処方線量と線量分布を調整するアプローチを採用している。low~favorable intermediate riskは35Gy/5回/7日間,unfavorable intermediate risk以上は36.25Gy/5回/7日間を原則とし,生検陽性箇所とMRI上描出される病変部位には可及的にSIBを行っている。線量増加された領域の平均線量は110%,最大線量は120%程度になることが多いが,boostを行う領域とリスク臓器との位置関係に線量増加の程度は左右される(図3)。さらに,PTVと直腸・膀胱そのものの重複領域は処方線量の90〜100%,PTVと直腸・膀胱・尿道にマージンを3mm付与した領域との重複領域は処方線量の98〜107%に抑えることで,がんの制御と毒性の低減の両立を図っている。
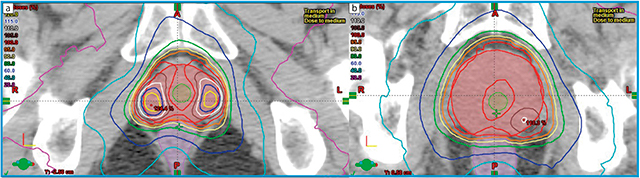
図3 前立腺に対するSIB-SBRTの線量分布
aは前立腺両葉のMRIで描出される病変に対してSIBを行った症例。リスク臓器の線量を抑えつつ,病変部位の平均線量は処方線量の114%,最大線量129%のSIBを行った。一方で,bのようにboostを行う領域が前立腺背側に寄っていると,尿道と直腸の線量を制約内に抑えるために,あまり線量は上がらない傾向がある。
“RapidArc”の利点
われわれは,以前よりバリアンメディカルシステムズ社製「CLINAC iX」によるRapidArcを用いて前立腺がんの通常分割照射を行っていた。そのため,前立腺がんに対するSBRTが保険収載された際も,照射技術面の抵抗感なく導入が可能であった。放射線治療計画装置「Eclipse」によるRapidArcの治療計画は,シンプルな考え方でoptimizationを行えるため,上述のように頭に思い描いた線量分布を作ることが可能である。また,定位放射線治療専用機に比べて照射時間も短い点や,CBCTで前立腺だけでなく膀胱や直腸を含めた消化管の状態を確認して照射ができることも利点である。
●参考文献
1)Katz, A. : Stereotactic body radiotherapy for low-risk prostate cancer ; A ten-year analysis. Cureus, 9 : e1668, 2017.
2)Alayed, Y., Cheung, P., Pang, G., et al. : Dose escalation for prostate stereotactic ablative radiotherapy(sabr); Late outcomes from two prospective clinical trials. Radiother. Oncol., 2018(Epub ahead of print).
3)Gomez, C.L., Xu, X., Qi, X.S., et al. : Dosimetric parameters predict short-term quality-of-life outcomes for patients receiving stereotactic body radiation therapy for prostate cancer. Pract. Radiat. Oncol., 5, 257〜262, 2015.
4)Boike, T.P., Lotan, Y., Cho, L.C., et al. : Phase Ⅰ dose-escalation study of stereotactic body radiation therapy for low- and intermediate-risk prostate cancer. J. Clin. Oncol., 29, 2020〜2026, 2011.
5)Kotecha, R., Djemil, T., Tendulkar, R.D., et al. : Dose-escalated stereotactic body radiation therapy for patients with intermediate- and high-risk prostate cancer ; Initial dosimetry analysis and patient outcomes. Int. J. Radiat. Oncol. Biol. Phys., 95, 960〜964, 2016.
6)Aluwini, S., van Rooij, P., Hoogeman, M., et al. : Stereotactic body radiotherapy with a focal boost to the mri-visible tumor as monotherapy for low- and intermediate-risk prostate cancer ; Early results. Radiat. Oncol., 8, 84, 2013.
