VARIAN RT REPORT
2018年11月号
ここまでできるがん放射線治療シリーズ No.9
慶應義塾大学病院でのPortal Dosimetryの使用経験
大野 真里(慶應義塾大学病院放射線技術室) / 深田 恭平[慶應義塾大学医学部腫瘍センター(放射線治療部門)]
はじめに
“Portal Dosimetry(PD)”は,バリアン社の放射線治療計画装置である「Eclipse」と同社のリニアック付属のelectronic portal imaging device(EPID)を利用して,IMRTの線量分布検証を行うQAシステムである。Eclipseで予測フルエンス分布を計算し,実際にEPIDに照射されたフルエンス分布と比較することで線量検証を行う。
PDはファントムなどの設置が不要であり,高い空間分解能で効率的に線量検証を行うことができる。一方で,従来の検証方法とは異なり,吸収線量での評価はできず,また,ターゲットやリスク臓器の線量評価はできないといった違いがあることに注意が必要である。
当院では,2015年よりバリアン社製リニアック「TrueBeam(Ver. 2.5)」でPDを一部の患者の線量検証に使用している。以下に,使用に当たり取得した物理データと臨床運用について述べる。
コミッショニングと検証について
PDのシステムを使用するに当たり,フルエンス予測アルゴリズムであるportal dose image prediction(PDIP)へのビームデータ登録およびシステム全体の基礎的な特性の検証を行った。
1.ビームデータ登録
PDIPには,最大照射野の対角プロファイル(off-center diagonal:OCD)と出力係数(output factor:OPF),およびバリアン社指定のピラミッド型の照射野(図1)を登録した。OCDはすでにほかのアルゴリズムに登録する目的で測定したものがあったので,それをそのままPDIPへの登録に使用した。OPFに関しては,EPIDを使って各エネルギーに対して49種類の照射野を測定する必要がある。当院では,6,10MVとflattening filter free(FFF)の6,10MVを合わせた4種の測定を2台のリニアックに対して行った。各エネルギーにつき1時間程度の測定時間が必要であったので,測定には合計で約8時間を要した。ピラミッド型照射野の測定も含めて,PDIPの登録に必要なデータ取得にかかった時間を合わせても,測定時間は10時間程度であった。

図1 PDIPに登録するピラミッド型照射野
EPIDで撮像した一例。PDを使用するためには,このデータを登録する必要がある。ここからCUを計算するためのカーネルを得る。
2.PDの基礎特性の検証
PDIPにビームデータが登録されるとPDの使用が可能となるが,当施設ではEPIDの基礎特性を知るために別途次に述べる検証を行った。
まず,照射monitor unit(MU)とpotal doseに当たるcalibration unit(CU)の直線性を確認した。すべてのエネルギーで,通常の治療で使用するMU値に対して十分な直線性が確認できた。次に,正方形の照射野をさまざまなガントリ角から照射して,EPID画像のオフセットとガントリ角の関係を調査した。正方形照射野の画像上のオフセットは,すべてのガントリ角度に対して0.5mm以内,またEPID平面上での回転は0.2°以内であることが確認されたが,オフセットが系統的であったことから,当施設では解析時に位置補正を行うことにしている。さらに,multi-leaf colimator(MLC)を用いてtongue&groove(T&G)効果が発生するような照射野を作成してPDIPの予測画像と比較した(図2)。PDIPはT&G効果も考慮して予測画像を作ることがわかった。また,この予測画像の測定値とのT&G部分の差異は,実際の線量計算に用いる計算アルゴリズムの計算グリッド(PDIPではなくAAAやAcurosXBの方)を小さくすることで縮小することが確認された。最後に,MLCを全閉した照射野を作り,leafのtransmissionを確認した。EPIDではノコギリ状の線量の高低が測定されたのに対し,PDIPはinter/intra-leaf transmissionに関しては平坦な予測値を返すにとどまった(図3)。
また,aS1000などのイメージャを用いたEPIDの測定では,アームの後方散乱が測定値に大きく影響を及ぼす可能性が示唆されていたが,本研究で用いたaS1200を使った測定では,Miriらの文献にあるとおり特段の補正を必要としなかった1)。
以上の基礎特性を考慮した上で,臨床での運用を検討した。
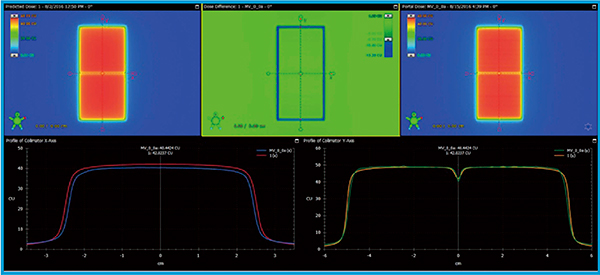
図2 PDIP予測画像とEPID取得画像の比較
上段左がPDIPによるpredicted dose,上段右がEPIDによる測定,上段中央が差を表す。下段左はLR方向,下段右はSI方向のプロファイルを比較したもの。SI方向プロファイル中央付近にT&G効果が現れているのがわかる。
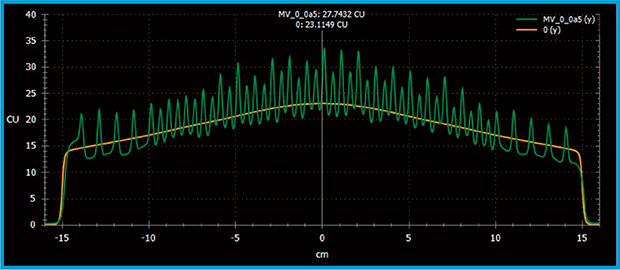
図3 MLCを全閉した時のプロファイル
MLCを全閉し,MLC動作方向と垂直な方向のプロファイルを測定した。EPIDによる測定では山谷状のMLCのtransmissionが確認できるのに対し,PDIPによるpredictionはこれらの平均値を返す結果となった。
臨床運用
PDによる線量分布検証は,EPIDに直接照射を行うため,ファントムなどを設置する手間が不要であり,ほかの手法に比べて短い時間で検証作業を行うことが可能である。VMAT検証の測定に要する時間は5分程度で,検証結果の解析も数分で終了する。また,解析結果はバリアン社製の放射線治療データ管理システム「ARIA」内で自動的に患者に紐づけられて一元管理されるため,容易に参照可能である。
当院での運用であるが,IMRTの検証のうち前立腺のプランに対してはPDを,そのほかの部位に対しては多次元検出器を使用している(図4)。後者は通常,プラン完成後3日間の検証期間を設けているが,至急の治療開始が必要な場合はPDで検証し,治療を開始することがある。その場合は,治療開始後数日以内のできるだけ早いタイミングで,多次元検出器による検証を追加する運用方針をとっている。当院のIMRTの線量検証の作業は,多次元検出器を使ったものは医学物理士が,PDは診療放射線技師が行っている。PDを診療放射線技師が行うことのメリットは,検証が短時間ですむ利点を生かし,患者の治療の合間にタイミングを見計らって検証を行うことができる点であり,このことは医学物理士の検証業務の負担軽減にも貢献している。一方で,PDの解析には,相対線量や絶対線量,位置補正の有無,γ解析のパラメータ,ノーマライズの方法など,施設で選択すべき項目が多い。複数名が解析に携わる場合には,解析者間で結果に差が生じないよう,これらの項目を統一しておくことも重要である。
PDを使うことで短時間で効率的に検証を行うことが可能であるので,突然のプラン変更にも柔軟に対応することができ,今後いっそう広まるであろうadaptive radiotherapyや,緊急照射においてIMRTを用いる高精度放射線治療にも対応できるツールであると考える。
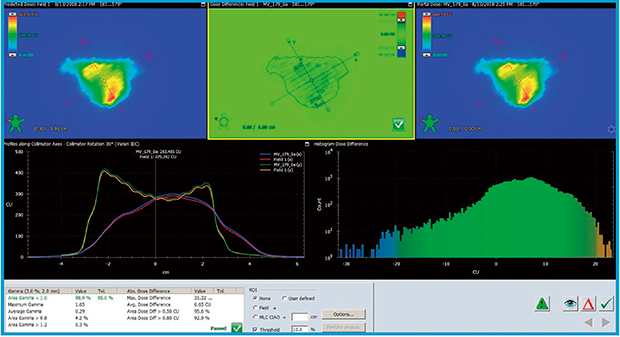
図4 前立腺PDの検証例
上段:左は治療計画装置で計算された予測フルエンス分布,右は実際にEPIDで実測したフルエンス分布,中央は予測と実測のフルエンス分布の線量差。
下段:左はコリメータ軸方向のX-Yプロファイル,右は予測と実測のフルエンス分布の線量差ヒストグラム。
γ解析は許容値γ≧95,クライテリア3%/2mm,thresholdは10%とし,ノーマライズは絶対値を用い,位置補正はローテーションも含めて行っている。
●参考文献
1)Miri, N., Keller, P., Zwan, B.J., et al. : EPID-based dosimetry to verify IMRT planar dose distribution for the aS1200 EPID and FFF beams. J. Appl. Clin. Med. Phys., 17, 292〜304, 2016.
