VARIAN RT REPORT
2018年6月号
ここまでできるがん放射線治療シリーズ No.5 特別企画:SBRT治療実績世界トップクラスの病院に聞く臨床アップデート
2)肝臓に対するRapidArc ─70% isodose処方法を用いた体幹部定位放射線治療
武田 篤也/鶴貝雄一郎/奥 洋平(大船中央病院放射線治療センター)
はじめに
肝臓に対する体幹部定位放射線治療(stereotactic body radiation therapy: SBRT)は,前号で述べた肺の場合とは異なり,いまだエビデンスの低い治療とみなされている。しかし,SBRTの患者にやさしい治療,安全な治療という特長は,肝臓の腫瘍に対しても当てはまる。今後,その特長を生かして適切な治療を行い,治療成績を報告していけば,SBRTは必ずや肝臓腫瘍治療の大きな一翼を担うと信じている。
肝細胞がんに放射線治療を行う際の注意点
肝臓は,肺に続き大きな臓器であるが,それでも肺の半分以下の容量である。正常肝であれば,右葉切除術にて肝臓の2/3を切除可能であり,切除後に組織の再生も起こる。一方で,慢性肝炎,肝硬変患者では,肝臓腫瘍に対する治療耐用性が低い。そのため,背景肝の機能を考慮して治療戦略を立てることが重要である。
肝細胞がん患者の背景肝には,ほとんどの場合慢性肝炎,肝硬変が存在する。肝硬変患者では,もともとの肝機能が低いばかりか,組織の放射線感受性も高くなるため,放射線治療による毒性も強く出現する。放射線治療後の肝臓には,高線量領域に一致して画像変化(focal liver reaction:FLR)が生じる。FLRは,単純CT,MRIでは淡い低濃度(信号)に描出され,門脈相から遅延相では淡い造影効果を呈し,肝細胞相では低信号として描出される。これは,放射線治療による肝障害を来している範囲が描出されていると考える。肝細胞がんに対するSBRT後のFLRを解析すると,Child Pugh分類A患者のFLRの閾値が30Gyであるのに対し,Child Pugh分類B患者の閾値は25Gyと低いことが判明した1)。また,肝細胞がんは肝内再発しやすい疾患である。報告では5年以内の肝内再発率は6割を超える。そして,肝細胞がん治療の特徴として,新たな肝細胞がんが出現した場合には,初発の場合と同様に,肝細胞がんのステージングと肝機能を鑑み,最適な治療方針を立てることとなっている。そのため,肝細胞がん治療では,腫瘍制御と肝機能温存の相反する2つの課題の両立が肝心である。
肝臓に最適な線量処方法に対する研究
われわれは,肺腫瘍に対するSBRTでは60% isodose曲線を計画標的体積(PTV)にフィットさせた治療法が最も効率的であると報告した。そこで,肝腫瘍に対する場合も同様に解析した。肝臓は軟部組織であり,腫瘍制御より肝機能温存を優先させることを考慮して,70% isodose曲線をPTVにフィットさせた治療法が最も効果的であるとした2)。
初発孤立性肝細胞がんに対するSBRTの多施設共同前向き試験(STRSPH study)を開始するに当たりdummy runを行った。その際に最初に指定された線量処法は,PTVのD95に対して40Gyを投与することであった。大船中央病院は70% isodose処方を採用していたが,他施設はPTV内を均一にする方針であったため,同じ線量処方でも施設間格差が大きいことがわかった。70% isodose処方では,肉眼的腫瘍体積(GTV),PTVに高線量照射されているものの,肝臓の線量は増加していない3)(図1)。この結果からも,70% isodose処方が効率的であることがわかる。そこで,STRSPH studyでの線量規定に70% isodose処方が加わった。
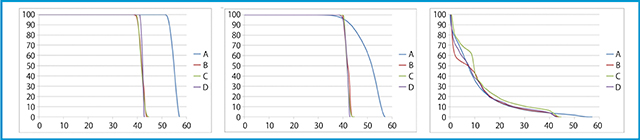
図1 STRSPH studyのdummy runにおける各施設の線量容積ヒストグラム(DVH)比較
左よりGTV,PTV,肝臓のDVH。Aが大船中央病院。
“RapidArc”の導入
われわれは,以前より多軌道回転原体照射を用いてSBRTを行っていた。そのため,バリアンメディカルシステムズ社製の「CLINAC iX」が導入され,RapidArc(VMAT)が可能となった際に,抵抗なくnon-coplanar RapidArcへ治療方法を変更した。RapidArc導入に伴い局所制御率も高まり,リスク臓器に近接する腫瘍にも適応を広げることができるようになったと実感している(図2〜4)。
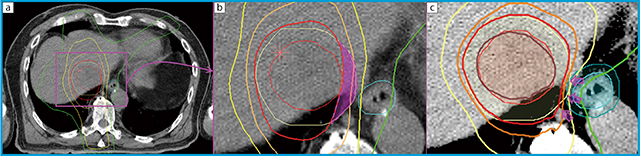
図2 肝細胞がんに対するSBRTの線量分布の一例(食道近接例)
a,bは,初回治療時の多軌道回転原体照射+固定照射による線量分布である。病巣が食道に近接しているため,食道への高線量照射を懸念して,食道近傍のPTVへの線量投与が不十分となった。この症例は1年を待たずに局所再発させてしまった。cはRapidArcにて再計画を行った線量分布図である。食道近傍まで高線量投与が可能である。この線量分布で照射をしていれば再発させないですんだかもしれない。悔やまれる症例である。 内側の○:GTV,○:PTV,等線量曲線は外側より10Gy(○),20Gy(○),30Gy(○),40Gy(○)(処方線量),45Gy(○)。
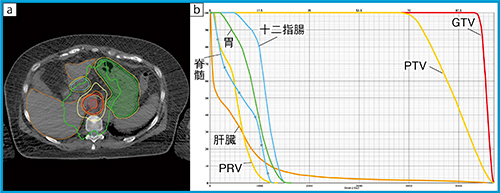
図3 肝細胞がんに対するSBRTの線量分布の一例
(胃,十二指腸,脊髄近接例:病巣はS1に存在する肝細胞がん)
aの内側の○:GTV,○:PTV,等線量曲線は外側より11.4Gy(○),22.9Gy(○),34.3Gy(○),40Gy(○)(処方線量),51.4Gy(○)。リスク臓器である胃(○),十二指腸(○)にそれぞれ3mmを付与して計画リスク臓器体積(PRV)としている。DVH(b)では,右側よりGTV(ー),PTV(ー),十二指腸(ー),胃(ー),脊髄(ー),PRV(胃と十二指腸合算+3mm)(ー),肝臓(ー)。
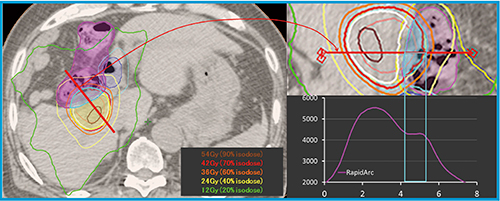
図4 肝細胞がんに対するSBRTの線量分布の一例(十二指腸,大腸近接例) 大船中央病院では,消化管近傍の肝細胞がんに対して42Gy/14回の分割照射を行っている。処方法としては,消化管PRVとPTVが重複する領域は42Gyに抑えつつ,重複しない領域に対しては70% isodose曲線と一致させるようにしている。また,消化管PRVの最大線量は50Gyを超えないことにしている。左図の赤線の線量プロファイルを右図に示している。RapidArcを用いることにより,消化管PRVとPTV重複領域への線量を42Gyに抑えつつ,重複しない領域への線量が増加している。また,消化管では可及的に線量が抑えられている。このように,RapidArcは放射線治療医の要求に応じた線量分布を作成可能にしている。 大腸(○),十二指腸(○),PTV(○)。等線量曲線は外側より12Gy(○),24Gy(○),36Gy(○),42Gy(○)(処方線量),54Gy(○)。
肝細胞がんに対するSBRTの治療成績
大船中央病院では,肝細胞がんに対するSBRTの単施設第2相試験を行った。対象は腫瘍径1〜4cmの孤立性肝細胞がんであり,脈管浸潤症例,他治療再発後救済症例を含んでいる。その結果,3年局所制御率は96%と高率であった4)。また,初発孤立性肝細胞がんを解析した後方視的研究では,3年全生存率は73%であり5),BCLC stage 0-A期に対する根治的治療に匹敵する成績であった。
●参考文献
1)Sanuki, N., Takeda, A., Oku, Y., et al. : Threshold doses for focal liver reaction after stereotactic ablative body radiation therapy for small hepatocellular carcinoma depend on liver function ; Evaluation on magnetic resonance imaging with Gd-EOB-DTPA. Int. J. Radiat. Oncol. Biol. Phys., 88, 306〜311, 2014.
2)Oku, Y., Takeda, A., Sanuki, N., et al. : Stereotactic ablative body radiation therapy with dynamic conformal multiple arc therapy for liver tumors ; Optimal isodose line fitting to the planning target volume. Pract. Radiat. Oncol., 4, e7〜e13, 2014.
3)Eriguchi, T., Takeda, A., Oku, Y., et al. : Multi-institutional comparison of treatment planning using stereotactic ablative body radiotherapy for hepatocellular carcinoma - benchmark for a prospective multi-institutional study. Radiat. Oncol., 8, 113, 2013.
4)Takeda, A., Sanuki, N., Tsurugai, Y., et al. : Phase 2 study of stereotactic body radiotherapy and optional transarterial chemoembolization for solitary hepatocellular carcinoma not amenable to resection and radiofrequency ablation. Cancer, 122, 2041〜2049, 2016.
5)Takeda, A., Sanuki, N., Eriguchi, T., et al. : Stereotactic ablative body radiotherapy for previously untreated solitary hepatocellular carcinoma. J. Gastroenterol. Hepatol., 29, 372〜379, 2014.
