VARIAN RT REPORT
2017年8月号
No.8 肝臓癌:技術編
広島大学病院:肝臓癌に対する定位放射線治療の現状 ─ 技術的ポイント
河原 大輔1)/中島 健雄1)/大野 吉美1)/木村 智樹2)/永田 靖2)(1)広島大学病院診療支援部放射線治療部門 2)広島大学病院放射線治療科)
はじめに
体幹部定位放射線治療(stereotactic body radiation therapy:SBRT)とは,比較的小さな肺,肝臓の腫瘍に対して,多方向から高い位置精度を保ちながらピンポイントで大線量照射を行う高精度放射線治療技術である。肝臓では肝細胞癌(hepatocellular carcinoma:HCC),または転移性肝腫瘍に対してSBRTが用いられることが多い。近年では,複雑な照射技術であるIMRT(intensity modulated radiation therapy)やVMAT(volumetric modulated arc therapy)で行われることもある。本稿では,SBRTを行う上で問題となる呼吸性移動対策,およびSBRTのVMAT化を推し進めている当院の経験について述べる。
呼吸性移動対策・位置照合
肝臓においてはターゲットの呼吸性移動が大きいため,その対策を講じる必要性がある。方法としては,ある呼吸位相でのみ照射する呼吸同期照射,呼吸を一定の位置で停止させて照射する呼吸停止照射,また,近年ではターゲットの動きを追いかけて照射を行う追尾照射なども行われており,どの方法を選択するかは施設の所有する装置やポリシーによりさまざまである。
当院では,肝臓に対するSBRTにおける呼吸性移動制御の第一選択は,「abches」(エイペックスメディカル社製)を使用した安静時呼気停止である。これは,われわれの過去の研究1)で報告したが,安静時呼吸停止のintrafractional errorは呼気時の方が吸気時に比べて小さいためである。位置照合においては近年,kV imagingやcone beam CT(CBCT)などのIGRT(image guided radiotherapy)システムが普及しており,肺腫瘍の位置確認は比較的容易に可能だが,肝臓では組織間コントラストに乏しいため,腫瘍の位置確認が困難である。当院では,SBRT前に肝動脈化学塞栓術(TACE)を行う場合が多く,集積するリピオドールがSBRTの際にも残存しているため,リピオドールの位置を腫瘍の位置とみなしCBCTで位置照合を行っている(図1)。リピオドールが残存しない場合,横隔膜面を基準とした位置照合を行っている。過去の研究において,われわれは横隔膜面照合および骨照合を行った場合のリピオドールの位置誤差を解析した2)。図2に結果を示すが,骨照合より横隔膜面照合を行った方が位置誤差は小さいことがわかる。われわれは,この解析により各照合法に必要なセットアップマージンを算出して,ターゲットの線量を担保している。
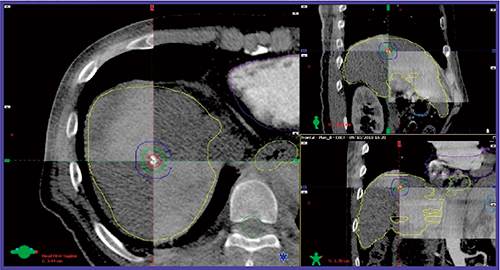
図1 肝臓癌SBRTにおけるCBCTによるIGRTの例
治療計画CTとCBCT画像を重ね合わせ,位置ズレの有無を確認している。
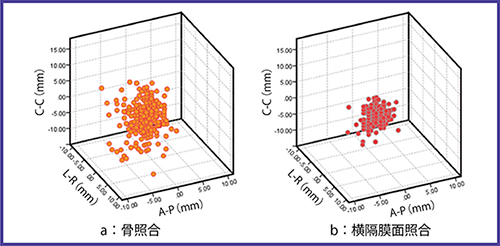
図2 骨照合(a),横隔膜面照合(b)を行った場合の腫瘍とみなしたリピオドールの位置誤差
VMATによるSBRT─当院での経験
当院では,2017年度よりSBRTのVMAT化を推し進めている。SBRTの品質管理においては,位置精度などの機械的精度および独立計算による線量の検証を行っていたが,VMATでは患者プランの検証を測定ベースで行うことにした。その上で,治療計画装置,線量計を使用した実測において,われわれが注意した点を紹介する。
治療計画装置において過去に小照射野の出力係数の確認を行ったが,図3に示すように,小照射野部分(1cm×1cm)での測定やモンテカルロ計算の結果と比較し5%以上の差が生じた3)。これは,治療計画装置が入力データから出力係数を外挿した小照射野領域であった。以上から,小照射野における出力係数などは,臨床に使用可能か事前に評価する必要がある。
面線量測定は,フィルム,検出器による測定など方法はさまざまである。当院の二次元検出器では,検出器間隔が1cmと大きいため照射野内の測定点が少ない。そのため,小照射野の評価が困難であるため,線量測定用フィルムは分解能が高い「GAFCHROMIC EBT- XD(EBT-XD)」(ベリタス社製) を使用して検証を行うこととした。EBT-XDは高線量域まで使用可能であり,SBRTに推奨されたフィルムである。図4に,事前検証として行ったコールドランのガンマ解析の結果を示すが,(線量差/DTA)=(3%/3mm) を判定基準として97%以上であり,良好な結果を示した。
近年では,高線量率で照射可能なflatterning filter free(FFF)ビームが使用されるようになり,大線量を投与しなければならないSBRTに有用とされている。しかし,FFFビームは平坦な線量プロファイルでないため,線量計の体積が大きいと有感体積の大きさによって線量の見積もりが異なる。これは体積平均効果と呼ばれる。Pinpoint線量計とファーマ型線量計の体積平均効果について,6X FFF ビームで約0.4%,10X FFFビームで約0.7%であったことが過去の研究で報告されている4)(図3)。
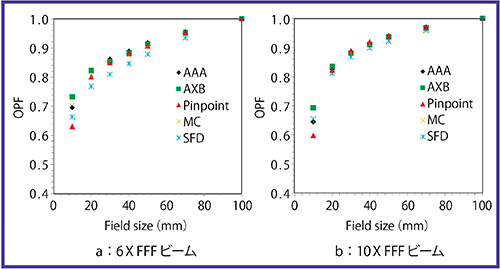
図3 6X FFFビーム(a)と10X FFFビーム(b)を使用した小照射野出力係数の検証
AAA, AXB〔治療計画装置「Eclipse」(バリアンメディカルシステムズ社製)の計算アルゴリズム〕,Pinpoint(電離箱線量計),MC(モンテカルロ計算),SFD(半導体線量計)の比較
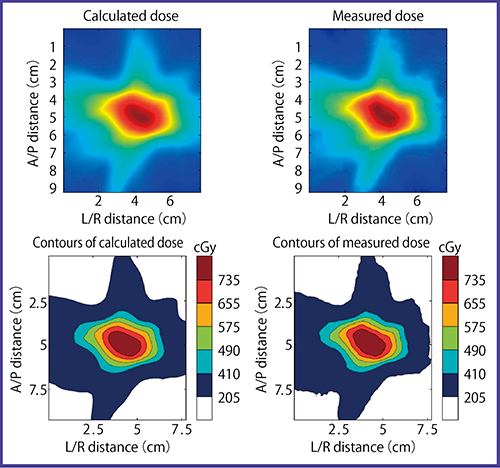
図4 フィルムによる患者プラン解析結果の一例
SBRTの今後─技術的課題
近年の治療計画装置では,ボルツマン輸送方程式やモンテカルロ法を用いた線量計算アルゴリズムなどが一般化し,精度の高い線量計算が可能である。しかしながら,TACE後に残存するリピオドールなどのように治療計画装置が考慮していない物質においては,既存の計算アルゴリズムでは吸収線量を正しく計算できない5)(図5)。また,呼吸性移動をセットアップマージンに含んだ計算は行えるが,呼吸性移動に伴う線量分布の変化は現在のところ困難である。
近年では,SBRTの処方法を腫瘍中心に対して設定する方法(アイソセンタ処方)から,planning target volume(PTV)の95%に照射された線量で評価する方法(D95%処方)など,セットアップマージンに対して処方線量を担保する方法に移行していることから,線量計算アルゴリズムの精度が直接処方線量に影響する。不均質領域の線量計算精度の向上,従来の三次元照射に呼吸性移動などの時間的要素を加味した四次元治療計画を行うことが,正確かつ堅牢性(ロバスト性)の高い線量分布の提供につながると考える。
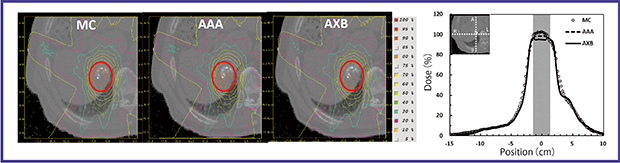
図5 リピオドールが残存した患者CT画像におけるモンテカルロ計算とEclipseの線量計算アルゴリズムであるAAA,AXBで計算した線量分布の比較
●参考文献
1)Kimura, T., Hirokawa, Y., et al. : Reproducibility of organ position using voluntary breath-hold method with spirometer for extracranial stereotactic radiotherapy. Int. J. Radiat. Oncol. Biol. Phys., 60・4, 1307〜1313, 2004.
2)Kawahara, D., Ozawa, S., et al. : Availability of applying diaphragm matching with the breath-holding technique in stereotactic body radiation therapy for liver tumors. Phys. Med., 32・4, 557〜561, 2016.
3)Kawahara, D., Ozawa, S., et al. : Evaluation of beam modeling for small fields using a flattening filter-free beam. Radiol. Phys. Technol., 10・1, 33〜40, 2017.
4)Sudhyadhom, A., Kirby, N., et al. : Preferred dosimeter size and associated correction factors in commissioning high dose per pulse, flattening filter free x-ray beams. Med. Phys., 43・3, 1507, 2016.
5)Kawahara, D., Oawa, S., et al. : Dosimetric Impact of Lipiodol in Stereotactic Body Radiation Therapy on Liver after Trans-arterial Chemoembolization. Med. Phys., 44・1, 342〜348, 2017.
