VARIAN RT REPORT
2017年9月号
No.9 肺癌:臨床編
北里大学病院:肺癌における放射線治療の現状
早川 和重(北里大学医学部放射線科学放射線腫瘍学)
はじめに:肺癌放射線療法の役割
肺癌の放射線治療には,根治治療として,(1) 切除不能非小細胞肺癌の胸部放射線照射,(2) 術前・術後照射,(3) 小細胞肺癌の胸部照射,(4) 小細胞肺癌の予防的全脳照射(prophylactic cranial irradiation:PCI)があり1),緩和治療として,(5) 広範囲な腫瘍進展・遠隔転移に伴う症状の緩和や延命を目的とした姑息・緩和照射などがある2),3)。また,分子標的薬や免疫チェックポイント阻害薬の登場により,最近ではIV期であっても抗癌薬物療法に奏功した後の少数病巣の残存(oligometastasis)や孤立再発例(oligo-progression),あるいは原発巣制御後の少数個転移例(oligo-recurrence)に対して積極的に局所放射線治療を追加しようとする考え方が議論されている。
肺癌(胸部)に対する放射線治療計画
治療計画用CT画像の取得
放射線治療計画はCTシミュレーションによる三次元治療計画装置を用いて行い,呼吸性移動が5mm(特に10mm)以上予測される場合には四次元CT画像を取得するが,定位照射(SRT)例では全例で四次元CTを撮影する。局所進行肺癌では,自由呼吸下と呼気時,吸気時の画像で計画することもある。
無気肺など二次陰影を伴う腫瘍や転移リンパ節の判断が難しい症例では,直接PET/CT装置で治療計画画像を取得するか,PET画像を計画用CT画像にフュージョンして治療計画を行う。患者体位は原則,上肢を下ろした安静仰臥位で計画するが,SRT,多門照射の際には上肢を挙上させることもある。
呼吸性移動対策
呼吸性移動対策には,「TrueBeam」(バリアンメディカルシステムズ社製)に搭載された「Real-time Position Management(RPM)system」(図1)と,動体追跡システム「SyncTraX」(島津社製)を用いている。SyncTraXは腫瘍近傍に留置した金マーカをX線透視下で追跡し,決められた三次元位置を通過する時に照射する迎撃照射(待ち伏せ照射)装置である。
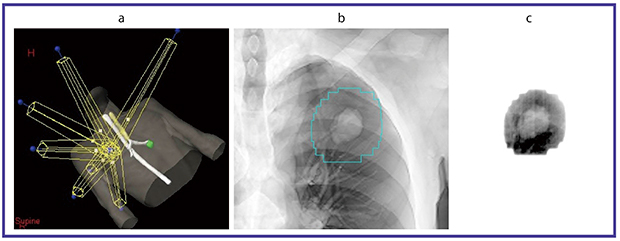
図1 RPMシステムによるSRTのmodel view(a),治療計画CTによるデジタル再構成画像(DRR)(b)と照射中のEPI像(後方からのportal image)(c)
症例は,70歳代,男性。右肺上葉の腺癌,T1aN0M0,IA期。non-coplanar 6門で48Gy/4回照射。
標的体積・リスク臓器の入力
原発巣と転移リンパ節を肉眼的腫瘍体積(GTV)として囲み,原発巣には浸潤部を含めて3~5mm程度のマージンを加えて臨床的標的体積(CTV)とし,リンパ節は領域に応じてCTVを設定する。局所進行癌では最大呼気,最大吸気相の移動範囲を確認し,internal margin(IM)を加えて体内標的体積(ITV)とし,適宜数ミリのリーフマージンをつけて照射野を決定する。縦隔転移リンパ節の肺側のマージンは十分とらなくても,治療経過とともにマージンが広くなることも想定して設定する。化学療法同時併用時には,CTVはGTVに近づけた照射野を用いている。
SRTの際にはGTV=CTVとし,四次元CT画像を参考に呼吸位相のどの範囲で照射するかを決定し,照射する各位相の画像上でGTVを囲み,それぞれのGTVを合わせた体積を治療時のITVとする。SyncTraXを用いる際には移動範囲3mmを許容することから,3mmの範囲でITVを決定する。
リスク臓器の入力は,三次元放射線治療計画システム「Pinnacle3」(フィリップス社製,日立社販売)搭載の“Auto-Segmentation”を用いて行っている。
症例1:Ⅲ期非小細胞肺癌に対する同時化学放射線療法
症例は,60歳代,男性。右肺上葉S3原発の腺癌,cT2aN2M0,ⅢA期で,シスプラチンとビノレルビンによる化学療法と胸部放射線治療60Gy/30回との同時併用療法を行った。治療効果は良好で経過観察中である(図2)。
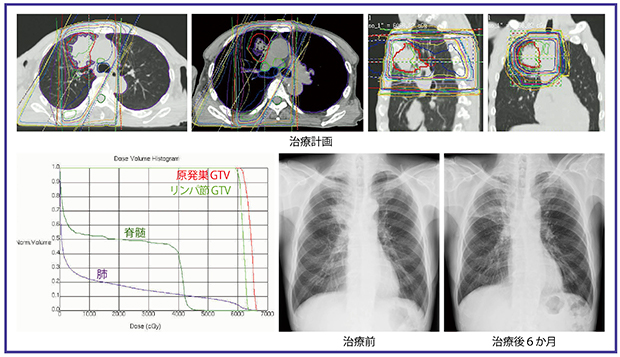
図2 症例1:同時化学放射線療法例
60歳代,男性。右肺上葉S3原発の腺癌,cT2aN2M0,ⅢA期。
症例2:IV期非小細胞肺癌の全身化学療法後の原発巣単独再発(oligo-progression)に対するSRT
症例は,60歳代,男性。右肺下葉原発の非小細胞肺癌(低分化で組織型不明),EGFR遺伝子変異del 19(+),cT4N3M1b(脳),Ⅳ期の診断で,2012年2月からエルロチニブを含む抗癌化学療法が施行された。治療により完全奏功に近い効果が見られ,経過良好であったが,3年後に右肺下葉に腫瘤影が増大してきたため,SRT 60Gy/10回を行った。SRT後,腫瘤影は縮小し,以後1年半再発なく経過している(図3)。
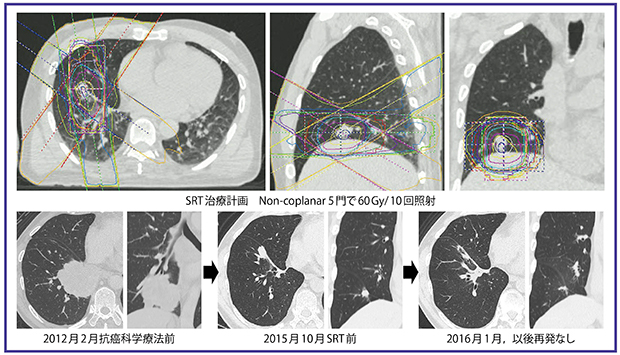
図3 症例2:oligo-progressionに対するSRTの例
60歳代,男性。右肺下葉原発の非小細胞肺癌(低分化で組織型不明),cT4N3M1b(脳),Ⅳ期で薬物療法後。 SRT治療計画はnon-coplanar 5門で60Gy/10回照射。
まとめ
肺癌に対する放射線治療では,呼吸性移動対策を伴う治療技術の高精度化と,全身療法の進歩とともに治療成績の向上が期待されている。今後は個々の患者背景や病態に応じた放射線治療を行うことが重要であろう。
●参考文献
1)日本放射線腫瘍学会:放射線治療計画ガイドライン2016.東京,金原出版,143〜165,2016.
2)早川和重:肺癌の放射線治療;根治治療と緩和治療.コンセンサス癌治療,13,75〜79,2014.
3)早川和重:肺癌に対する放射線治療の現況と展望. 臨床外科,67,986〜991,2012.
