セミナーレポート(富士フイルムヘルスケア)
第30回日本泌尿器内視鏡学会総会が2016年11月17日(木)〜19日(土)の3日間,ナレッジキャピタル コングレコンベンションセンター(大阪市)などを会場に開催された。18日に行われた株式会社日立製作所共催のイブニングセミナー5では,神戸大学大学院医学研究科腎泌尿器科学分野教授の藤澤正人氏を座長に,大阪市立大学大学院医学研究科泌尿器病態学病院講師の山﨑健史氏と神戸大学大学院医学研究科腎泌尿器科学分野特命准教授の日向信之氏が,「ロボット支援腎部分切除術における術中エコーアプローチの有用性」をテーマに講演した。
2017年3月号
第30回日本泌尿器内視鏡学会総会イブニングセミナー5 ロボット支援腎部分切除術における術中エコーアプローチの有用性
ロボット支援腎部分切除術における術中エコーの有用性
山﨑 健史(大阪市立大学大学院医学研究科泌尿器病態学)

当院では,2016年6月からロボット支援腹腔鏡下腎部分切除術(RAPN)を開始し,11月までに21症例22腎に実施した。また,2011年から現在までに腹腔鏡下腎部分切除術(LPN)を158症例に対して実施しており,この経験を基にRAPNを施行している。本講演では,RAPNにおける術中エコーの運用の実際,および日立製作所製超音波診断装置「ARIETTA 70」で使用可能な術中エコープローブ「L43K」の有用性について述べる。
LPNでの工夫とRAPNへの期待
LPNにて機能温存(阻血時間短縮,腎血流の温存),制がん性(切除断端陽性率低下),安全性(出血・仮性動脈瘤・尿瘻などの合併症の軽減)を達成するために,当院では,例えば腎動脈の阻血解除後に腎実質を縫合するearly unclamping法による阻血時間の短縮や,IO電極によるソフト凝固を行うことで合併症の軽減に努めてきた。また,腫瘍辺縁は5mm程度のマージンを確保し,腫瘍底についてはシーリングデバイスなどを用いた鈍的剝離を多用し,より少ないマージンを意識することで,不要な切り込みによる切除断端陽性や,血管損傷に伴う腎血流の低下を防ぐことを心掛けてきた。
一方,当院にて治療を行ったLPNの158症例についてRENAL Nephrometry Scoreで評価したところ,10点を超えるhigh complexity tumorの症例では腎血流の低下に伴う腎機能低下が予想以上に大きかった。そこで,こうした症例の治療成績を向上するために,RAPNが有用と考えている。
RAPNにおける術中エコーの活用
1.従来の術中エコープローブの課題
腹腔鏡下手術は視野が狭く,スペースの制限からエコープローブの操作性の自由度が低い。また,従来のエコープローブは可動性に制限があるため,挿入するポートや腫瘍の位置によってはプローブを当てづらく,正確な画像を得るのが困難である。そのため当院では,腫瘍が突出し,腎門部からも距離があるような症例については,術中エコーなしでも切除することがある。術中エコーである程度の見当をつけて正常な腎実質が見えるラインで切除すれば,腫瘍に切り込むことはなく,腎機能の低下や術後合併症の心配も不要と思われる。
一方,腫瘍が腎実質内に半分以上埋没し,主要な血管が腫瘍近傍に複数走行しているような症例では,上述したような切除の仕方では予想以上の腎血流低下や切除断端陽性,腎機能の大幅な低下につながりかねない。そのため,こうした腫瘍の場合は,腎実質のマージンをある程度残した上で,速やかに腫瘍底まで切除を進め,腫瘍に切り込まない範囲で可能なかぎり腫瘍を摘出するというイメージを持つことが重要である。しかし,従来の術中エコープローブでは,そこまでイメージできるほど十分な画像を得るのが困難だった。
2.ドロップイン型プローブ「L43K」の有用性
そこで,当院でRAPNの導入に伴い使用を開始したのが,鉗子で把持可能なドロップイン型プローブのL43K(図1)である。L43KはLPN用のプローブよりも先端が小さく,ケーブルが柔らかいためフレキシビリティに優れるほか,腫瘍の輪郭に沿ってしっかり押し当てられるので,より良好な画像が得られるようになった。このため,より正確に腫瘍の切除ラインをイメージすることができる。そのイメージを基にしたロボットの繊細な操作が加わることで,きわめて精緻な手術が可能になると考えている。

図1 ドロップイン型の術中エコープローブL43K
RAPNによるhigh complexity tumorの症例提示
症例1は,74歳,男性,5.1cmの左腎細胞がんである(図2)。腫瘍が半分以上埋没しているため,なるべく少ないマージンで速やかに腫瘍底まで切除し,その後切り上げていく。その際,前述のとおり適切な切除ラインをイメージすることが重要であり,術中エコーがきわめて有用である。L43Kを腫瘍にしっかりと押し当てることで従来よりもかなり明瞭な画像が得られ(図2右),また,プローブ先端は小さくても腫瘍全体のイメージを十分につかむことができる。本症例は,阻血時間は26分とやや長めであるが,残すべき血流はしっかりと残し,不要な尿路の損傷を防ぐことで術後合併症もなく,腎機能も血清クレアチニン濃度(s-Cre)が術前0.93mg/dLに対し術後1.01mg/dLと十分に保たれていた。
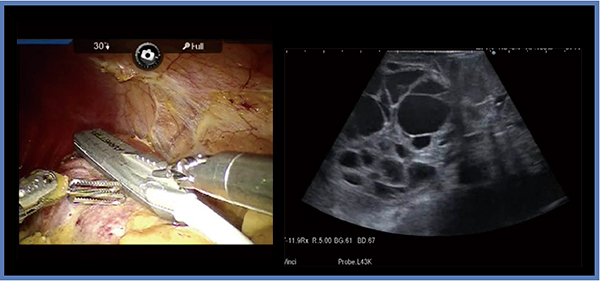
図2 症例1:左腎細胞がん(74歳,男性)
症例2は,47歳,男性,両側腎細胞がんである(図3)。本症例では左腎の4.7cmの腫瘍が腎門部にほぼ埋没しているが,このようなhilar tumorの切除にも,術中エコーが有用である。切除に当たっては,まず腎切痕よりアプローチして腎動静脈,腎盂から腫瘍をしっかりと剥離し,腫瘍の可動性が得られた時点で,エコー画像を基に切除ラインを確認し,腎実質を切除して腫瘍を切離する。その際,部位によって鈍的剥離と鋭的な切除を使い分けることで血管や尿路の不必要な損傷を防ぎ,安全に切除可能である。また,実質縫合の際,inner sutureを行うことで腎孟の縫い込みや腎血管の損傷が起きる可能性があるため,当院では基本的に一層のみで行っている。本症例は,両腎を一期的に手術したため,腎機能(s-Cre)が術前の1.17mg/dLに対し,術後1週目には2.19mg/dLと低下したが,術後4週目には1.36mg/dLにまで回復した。
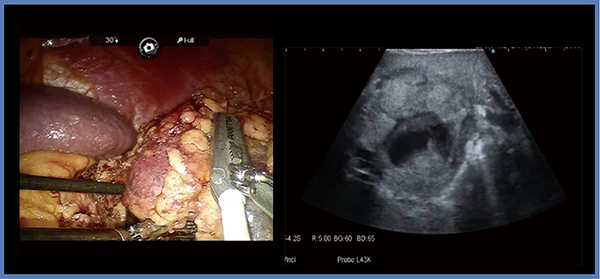
図3 症例2:両側腎細胞がん(47歳,男性)
症例3は,45歳,男性,2.3cmの右腎細胞がんである(図4)。腫瘍は完全に埋没しているが,症例2と同様のアプローチで切除を進めていく。本症例は背側に腫瘍があったため,腎の受動性を十分確保し,腎動静脈や腎盂をその走行が確認できるよう剥離しておくことで,安全な切除が可能となる。症例2と同様に腎盂,腎動静脈から腫瘍底をある程度剥離した後にエコーで腫瘍の位置を確認すると,腫瘍被膜まで十分剥離できていることが確認できる(図4右)。このような,LPNでは腎実質の欠損がかなり大きくなると思われる症例も,RAPNにて最小限のマージンで切除可能である。本症例も,縫合は腎実質一層のみとしている。阻血時間は17分と比較的短時間であり,腎機能(s-Cre)の低下も,術前が0.59mg/dL,術後が0.65mg/dLと最小限にとどめることができた。
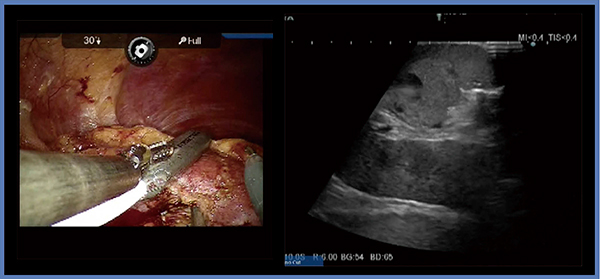
図4 症例3:右腎細胞がん(45歳,男性)
RAPNとLPNにおける周術期成績の比較
当院で施行したRAPN 21症例22腎,およびLPN 158例中hilar clampの113症例について周術期成績を比較したところ,手術時間や出血量,阻血時間に有意差は認められなかったが,腎機能の回復〔ΔeGFR(mL/min/1.73m2)〕はRAPNが3.97±5.1,LPNが10.77±8.3と,RAPNの方が良好であった。今後RAPNの症例が増えていけば,阻血時間にも差が出てくると考えられる。
まとめ
LPNの時代から一貫して,high complexity tumorの切除においては腫瘍底のマージンを限りなく少なくすることをめざして行ってきたが,鉗子の自由度の高いRAPNを導入し,より緻密な操作とドロップイン型のプローブなどを活用することで,最小限のマージンでの切除が可能となった。LPNと比較してRAPNでは,手術の精度が圧倒的に向上していると実感している。
山﨑 健史(Yamasaki Takeshi)
2002年 大阪市立大学医学部卒業。2011年 同大学院卒業。2013年 同大学院医学研究科泌尿器病態学病院講師。
- 【関連コンテンツ】
