次世代の画像解析ソフトウェア(AZE)
2015年4月号
No. 156 脊髄硬膜動静脈瘻に対するCTA術前支援画像の有用性について
金城 一史(社会医療法人友愛会 豊見城中央病院放射線科CT室)
はじめに
当院は救急体制の充実化のため,2012年5月に脳神経外科を新規に開設した。脳神経外科医2名による2013年度の手術件数は257件(血管内治療110件,開頭術88件,穿頭術38件,経鼻的術8件,その他13件)で,画像検査件数は頭頸部3D-CTA100件,脳アンギオ158件と増加した。サージカルビューを中心とした術前支援画像の処理を中心に考えた結果,ワークステーション(以下,WS)「AZE VirtualPlace 雷神」(AZE社製)を導入した。
今回,WS導入直後に行った脊髄硬膜動静脈瘻に対する3D-CTAの画像構築が,血管内治療の術前支援画像として有用だった症例を経験したので報告する。
患者背景
症例は71歳,男性。両下肢筋力低下と歩行困難による日常生活動作(ADL)低下を主訴に当院受診となった。既往歴として黄色靭帯骨化症・脊柱狭窄にて手術歴(胸髄・腰髄手術)があり,今回,脊髄MRIにて胸髄,腰仙髄の脊髄中心性髄内信号変化(硬膜動静脈瘻+,静脈うっ血性脊髄症s/o)を認め,MRIの脂肪抑制T2WIにてL1-2レベルの硬膜囊内左側寄りに,拡張,蛇行する脈管構造が疑われた(図1)。脊髄硬膜動静脈瘻(Dural AVF:以下,d-AVF)を見ている可能性があることから,確定診断を目的として3D-CTAの依頼となった。
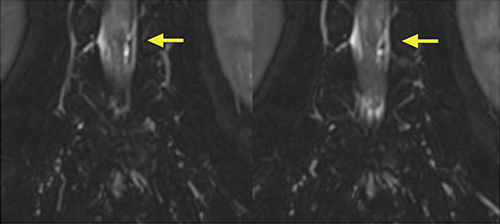
図1 脂肪抑制T2WI
脊髄硬膜動静脈瘻に対する3D-CTAの撮影条件
脊髄硬膜動静脈瘻とは,神経根の硬膜を栄養する根動脈と根静脈との間のシャントによるものであり,流入動脈血管1)をイメージした(図2)。撮影条件を考えるにあたり,Adamkiewicz動脈撮影を行った2例の撮影条件を参考とした(図3)。
2例ともC5から恥骨結合レベルまでの撮影範囲で,ボーラストラッキング法を用いて胸部上行大動脈にROI(200HU+5秒)を設定し,使用する管電圧は100kVpを選択した。大動脈血管のCT値を500〜600HUまで上昇させ,大血管から分岐する末梢までの血管を十分に濃染するため,low pitch helical scan(寝台移動速度を25mm/s)で,mAs値を担保しつつ後期動脈相を撮影し,体重比用量710mgI/kgにおいて良好な3D画像を得ていた。
今回のケースは,腹部大動脈から分岐する肋間・腰動脈から,分岐し流入する動脈血管,シャント,輸出静脈血管の走行確認と血管内治療による根治を念頭2)に置いた3D構築を最大の目的としている。単位時間あたりのヨード造影剤の注入量は30mgI/kg/sが望ましいことを主治医,放射線科医に伝え,ヨード造影剤の使用量と方法も含め十分な説明と同意の下に注入条件を決定した。
実際の撮影範囲はTh8〜恥骨結合までとされ,開始位置Th8レベルにボーラストラッキング法のROI(300HU+5秒)を設定した。大血管から分岐していく脊髄の末梢血管に造影剤が満たされている状態で撮影するため,大血管の造影剤到達ピークを長く保つことを考え,単位時間あたりの造影剤注入量を30mgI/kg/s×撮影時間24秒で720mgI/kgとした。よって,体重59kgにおけるヨード造影剤(イオヘキソール300)は,5.9mL/s(141mL:24秒+生食後押し35mL:6秒)30秒間注入プランとなった。撮影範囲は425mmで24秒間撮影であるため,寝台移動速度は18mm/sとなった。
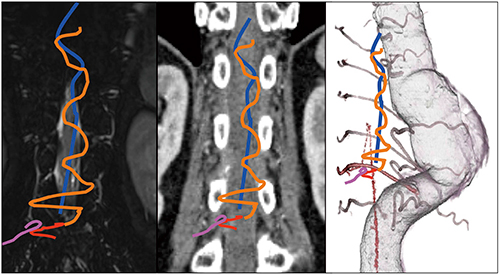
図2 d-AVFのイメージ画像
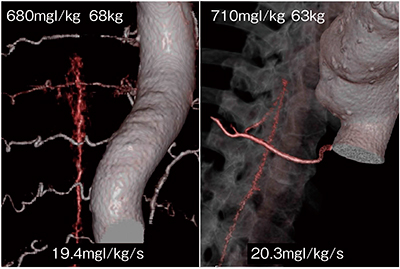
図3 Adamkiewicz動脈撮影の撮影条件
35秒注入固定の4.3mL/s(イオヘキソール300
150mL+生理食塩水後押し35mL)
撮影結果からIVRによる血管内治療まで
撮影終了直後はAZE社のWSは導入されておらず,神経内科による第一次カンファレンスでは,d-AVFが考えられる血管の蛇行はあるが,流入血管ははっきりしない状態であるとコメントされていた。検査終了の2週間後にAZE社のWSが導入され,非剛体サブトラクション処理を行ったところ,動静脈の画像が鮮明に描出された(図4,5)。脳神経外科医よりd-AVFを疑う3D画像であると指摘され,診断アンギオ画像と3D画像との一致する所見情報により,IVR治療が検討され,血管内治療のシミュレーションが行われた(図6)。
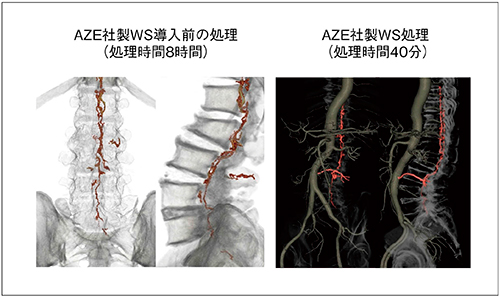
図4 AZE社製WS導入前と導入後の違い
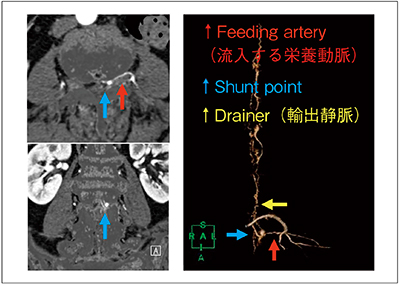
図5 AZE社製WSによる非剛体サブトラクション処理画像
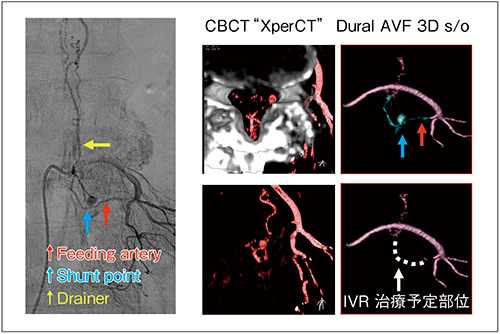
図6 診断アンギオから術前シミュレーションした3D画像
IVR治療の流れ
根静脈にシャントを形成するタイプがあるため,5Frシェファードフックカテーテルを左第3腰動脈に誘導して撮影すると,シャントに続く輸出静脈血管を認めた。Marathon/Tenrou10にてシャントを越えて輸出静脈血管まで誘導し,よく温めた20%NBCA0.1mLを注入したところ,DSAにてシャントおよび輸出静脈血管は描出されなくなった(図7)。
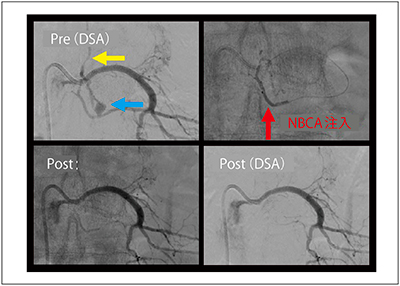
図7 IVRによる治療
まとめ
WS導入直後の処理でありながらも,d-AVFの細部血管に至るところの腰椎の分離を完全に近い状態で行えた非剛体サブトラクション処理は,3D画像による血管構築の理解を助けるIVR術前シミュレーションとして有用であったと考える。IVRの術中手技と治療に要する時間についても,全身麻酔下での治療室入室から退出まで73分,治療時間は36分で終了しており,WSの処理能力の高さが短時間で的確な治療を成功させるポイントの一つになっている。
治療後の患者は劇的な改善傾向を見せ,足が上がるようになり,立脚期に両膝完全伸展位での歩行が可能となった。半年後の経過観察においても,歩行速度も速くなり,MRIでのフォローでも再発なく経過良好と報告を受けている。現在は,WSのサブトラクション機能の詳細設定値と画像化に向けた検討を重ねている最中であり,できるかぎり造影剤を低減した3D画像化を目標としている。
●参考文献
1)山口昻一, 宮坂和夫 : 脳脊髄のMRI. 東京, メディカル・サイエンス・インターナショナル, 545~552,1999.
2)三宅 茂, 藤田敦史, 甲田将章・他 : NBCAを用いた塞栓術後に再発した脊髄動静脈瘻の1手術例. 脳神経外科ジャーナル, 14, 718〜722, 2005.
【使用CT装置】
SOMATOM Sensation 64(シーメンス社製)
【使用ワークステーション】
AZE VirtualPlace 雷神(AZE社製)
