2018-9-3
(株)日立産業制御ソリューションズ(以下,日立産業制御)は,医薬品の品質や安全性確保を目的に定められた国際的な基準GMP*1に基づく文書を電子化し,作成から管理,廃棄に至るまでの文書管理・検索を実現するGMP文書管理パッケージ「HITQUAA(ヒットキュア)」に,教育管理機能を追加した新バーション「HITQUAA V02-00」を,2019年1月から販売開始する。日立産業制御は,医薬品・医療機器業界をターゲットに,2021年度までに60社への製品導入をめざす。
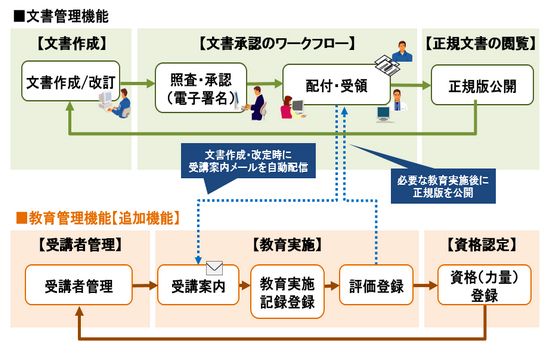
「HITQUAA V02-00」教育管理機能追加イメージ
医薬品・医療機器は人の生命や健康に直接関係することから,医薬品・医療機器製造業者は,最新版の手順書にのっとり,定められた製造・品質業務を適正に遂行し,規格に適合した品質を常に提供する責務がある。この職責を全うするために,製造従事者は,手順書に基づいた実務の教育訓練およびGMP教育を実施することがGMP省令で定められている。GMPは文書化・記録化が前提であることから,近年のGMP査察の強化などを背景に,製造従事者への教育管理と文書管理の連携ニーズが高まっていた。
そこで日立産業制御は,省令要件に従ってGMP文書を正確かつ効率的に管理することが可能な「HITQUAA」に,教育管理機能を追加した「HITQUAA V02-00」を開発した。本製品を活用することで,医薬品・医療機器製造従事者は,GMP省令に沿った適切なタイミングで教育を実施し,電子文書として記録できることから,教育の実施漏れを防止し,省令順守と医薬品・医療機器の品質・安全性の確保,教育管理業務の負担軽減が可能となる。
今後,日立産業制御は「HITQUAA V02-00」の拡販とともに,「HITQUAA V02-00」と日立産業制御が販売する品質イベント管理システム「TrackWise(トラックワイズ)」および日立グループが提供する各種ソリューションを連携することで,医薬品・医療機器業界における業務品質向上や迅速化などの業界ニーズに応えたソリューションをトータルに提供する。これにより,医薬品・医療機器の品質や安全性の維持向上,業務効率化に貢献していく。
*1 GMP(Good Manufacturing Practice):「医薬品及び医薬部外品の製造管理及び品質管理の基準」。各国がこれに準ずる基準を設けており,日本では厚生労働省が省令などで規定している。
●「HITQUAA V02-00」の特長
1.省令要件に従ってGMP文書を正確かつ効率的に作成・管理することが可能
GMP文書の作成から廃棄までのワークフローを構築し,文書の状態を正確に把握できる。文書の配付通知や公開,受領などの確認,文書の有効期限管理や電子署名による承認など,省令遵守に必要な機能や求められる高い信頼性を確保しており,管理業務の負担軽減を実現する。
2.教育の実施漏れを防止し,省令順守,品質と安全性の確保,管理業務負担の軽減を実現(追加機能)
GMP省令に沿い,文書作成・改訂時および受講者ごとの資格(力量)認定に必要な教育を一元管理することが可能。文書作成・改訂時には,文書の照査・承認後に教育対象者へ受講案内メールを自動配信するほか,教育実施後に正規版を公開するなどの機能により,教育の実施漏れを防止し,省令順守,品質と安全性の確保,管理業務の負担軽減を実現する。
「HITQUAA V02-00」に関する日立産業制御のWebサイト
http://info.hitachi-ics.co.jp/product/hitquaa/
品質イベント管理システム「TrackWise」に関する日立産業制御のWebサイト
http://info.hitachi-ics.co.jp/product/business_support/trackwise/tw01.html
●問い合わせ先
(株)日立産業制御ソリューションズ
http://info.hitachi-ics.co.jp/product/hitquaa/
