技術解説(フィリップス・ジャパン)
2023年3月号
Cardiac Imaging 2023 CT技術のCutting edge
循環器領域におけるフィリップスCTの技術動向
小川 亮[(株)フィリップス・ジャパンCTモダリティセールススペシャリスト]
2021(令和3)年,「人口動態統計月報年計(概数)の概況」1)によると,本邦における死因順位第1位は悪性新生物,第2位は心疾患(高血圧性を除く),第3位は老衰となっている。この中で,第2位の死因である心疾患は,1985(昭和60)年に脳血管疾患に代わり第2位となり,2021年には全死亡者に占める割合が14.9%と,全体的に見ても非常に高い死亡率となっている。その心疾患の大部分を占めるのが虚血性心疾患であり,CTを含む画像診断の役割は,病変の検出,治療戦略,術後評価など多岐にわたる。
「2021年度循環器疾患診療実態調査報告書」2)では,冠動脈の画像診断における心臓CTの検査件数は2019年時点で50万件を超え,侵襲的な冠動脈造影検査より多く施行されている。さらに,安定冠動脈疾患の診断と治療における「2022年JCSガイドラインのフォーカスアップデート版」3)では,古典的閉塞性安定冠動脈疾患における非閉塞性冠動脈疾患のrule outにおいて,心臓CTの有用性が示唆されている。しかし,コントロール不良の高心拍数(高HR)や心拍不整,また,高度石灰化,腎機能障害の患者には適さないなどの注意点も同時に記載されている。これらの問題点は,冠動脈を対象とする画像診断において,陽性的中率低下の大きな一因となり,その問題を改善することは,冠動脈の画像診断において非常に重要である。本稿では,これらの問題点を改善するフィリップスCTに搭載されたAIを含む画像再構成技術に加えて,さらなる確信度を高めた画像診断をサポートするスペクトラルイメージングについて,臨床症例を交えて紹介する。
■さまざまな心拍に対応する画像再構成アルゴリズム
1.不整脈に対応した画像再構成アルゴリズム
近年,不整脈患者は増加傾向にあり,R-R間隔が不均等な不整脈症例は,冠動脈のモーションアーチファクト,バンディングアーチファクトによって画質劣化が顕著となる。そこで,フィリップスがこれまで発表している64列以上のすべての機種には,この問題に対する画像再構成アルゴリズムが搭載されている。それらのアルゴリズムは,以下のとおりである。
(1) Beat to Beat Algorithm:不整脈によって心拍変動が出現した場合に,基準心拍の任意の心位相に自動補正することで,R-R間隔が異なる不整脈症例においても冠動脈の連続性が高くバンディングアーチファクトが少ない画像を提供することが可能となる。
(2) Adaptive multicycle reconstruction:画像再構成中にセグメント分割数と分割比率を自動可変処理することで,R-R間隔の変動を有する症例においても時間分解能の担保された診断精度の高い画像を得ることできる。
(3) Auto Arrhythmia Detection:心臓CT検査終了時に,本体コンソール上に不整脈によるアラートを表示することで,不整脈を見落とすことのない心電図編集を可能とする。
これらの技術は自動化されたアプローチであるため,撮影者の技量によらず,不整脈症例においてアーチファクトが少ない冠動脈の画像を取得することができる。図1は心房細動の症例である。このように,HRが50〜120bpmと心拍変動が大きな症例においてもアーチファクトの少ない診断能の高い画像が得られている*。

図1 不整脈に対応するBeat to Beat Algorithm,Adaptive multicycle reconstruction,Auto Arrhythmia Detectionを用いた心房細動(Af)症例
(画像ご提供:千葉西総合病院)
2.高HRに対応したAI画像再構成アルゴリズム「Precise Cardiac」
フィリップスは,前述の再構成技術に加え,AI技術を応用し,高HRによる冠動脈のモーションアーチファクトを低減することが可能なPrecise Cardiacを開発した。Precise Cardiacは,本体コンソール上で動作可能なアルゴリズムであるため,検査ワークフローを損なうことなく,日常臨床への適用が可能である。一般的な心臓CTにおける画像再構成法では,相対delay法あるいは絶対delay法で決定した心位相の投影データのみを画像再構成に用いる。一方,Precise Cardiacの画像再構成プロセスは,ターゲットとする心位相だけでなく,ターゲット近傍の位相データを使用し,その連続データの全ボクセルに対し,ベクトル解析による動きの推定と非剛体レジストレーションを行う。この一連の処理の中で,AIで事前に学習されたアルゴリズムが用いられている。図2の症例は,128sliceの「Incisive CT」で撮影されたHR:138の高HR症例である。撮影時の回転速度は0.35sと,従来ではモーションアーチファクトの影響により画質劣化が予測できる症例であるが,Precise Cardiacではモーションアーチファクトの影響が少なく,視認性の向上した冠動脈画像が得られている。

図2 AI画像再構成
Precise Cardiacを用いた高HR症例(HR:138bpm)
(画像ご提供:長野中央病院)
■確信度を高めた画像診断を提供するスペクトラルイメージング
近年,2つの管電圧からさまざまな画像を取得することが可能なdual energy CT(DECT)が臨床応用されている。フィリップスが開発したDECTは,2層検出器を用いた心電図同期撮影により,single energy CT(SECT)で課題となっていた循環器領域の症例に対して,従来画像と空間的・時間的ミスレジストレーションがないスペクトラルイメージングを用いることで,診断能を向上することが可能である。
1.高度石灰化病変における診断能向上
これまでのSECTにおいて,冠動脈の高度石灰化は,ブルーミングアーチファクトの影響により冠動脈狭窄率の過大評価を及ぼす原因となっている。しかし,2層検出器によるスペクトラルイメージングでは,エネルギーを40〜200keVで連続的に可変して表示することができる仮想単色X線(MonoE)を得ることができ,MonoE高keV画像を用いることで,ブルーミングアーチファクトの影響を低減することができる(図3)。これにより,高度石灰化を有する症例においても,より精度の高い狭窄率の評価が可能となる。

図3 高度石灰化症例
2.簡便なECV評価
近年注目されているextracellular volume(ECV)による定量的評価は,細胞外容積の広がりを反映した定量的指標となり,虚血性心疾患を含む心疾患において,重症度評価・リスク評価を行う上で有用である。スペクトラルイメージングの一つであるIodine densityでは,遅延造影1相のみの画像データからヨード密度値をダイレクトに算出することで,空間的・時間的ミスレジストレーションがないECV評価が可能となる。また,フィリップスのワークステーションである「IntelliSpace Portal(ISP)12」に搭載されたアプリケーションである「Multimodality Analysis」では,よりシンプルで簡便なECV評価を提供している(図4)。操作の簡単な概要は,ECVの選択→大動脈内でIodine値の正規化→各患者のヘマトクリット値を入力し,評価対象とする心筋内にROIを置くだけで,ECV値の表示が可能となっている。
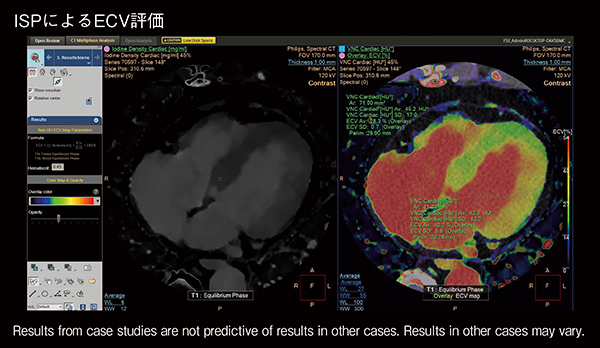
図4 スペクトラルイメージング+ISPによる簡便なECV評価
◎
本稿では,これまでの心臓CTの問題点として考えられる課題に対して,フィリップスのさまざまな循環器領域に特化した技術を紹介した。これらの技術は,より簡便で確信度の高い循環器領域の画像診断をサポートする技術であり,今後,心疾患における死因の抑止力の一助となることに期待する。
*結果は患者ごとに異なるため,すべての不整脈への対応を保証するものではありません。
●参考文献
1)令和3年(2021)人口動態統計月報年計(概数)の概況. 厚生労働省.
https://www.mhlw.go.jp/toukei/saikin/hw/jinkou/geppo/nengai21/dl/gaikyouR3.pdf
2)2021年度循環器疾患診療実態調査報告書. 日本循環器学会.
https://www.j-circ.or.jp/jittai_chosa/media/jittai_chosa2020web_1.pdf
3)日本循環器学会, 他 : 2022年JCSガイドラインフォーカスアップデート版安定冠動脈疾患の診断と治療.
https://www.j-circ.or.jp/cms/wp-content/uploads/2022/03/JCS2022_Nakano.pdf
問い合わせ先
株式会社フィリップス・ジャパン
〒108-8507
東京都港区港南2-13-37 フィリップスビル
お客様窓口:0120-556-494
受付時間:9:00~18:00
(土日祝祭日・年末年始を除く)
www.philips.co.jp/healthcare

