
ホーム
![]() inNavi Suite
inNavi Suite![]() フィリップスエレクトロニクスジャパン
フィリップスエレクトロニクスジャパン![]() Technical Note
Technical Note![]() PET/CT−OncologyのためのPET/CT―TOF
PET/CT−OncologyのためのPET/CT―TOF
2008年4月号
Abdominal Imagingにおけるモダリティ別技術の到達点
マーケティング本部核医学
本稿では,フィリップスPET/CTの腹部領域における技術到達点について報告する。 ■ TOFを実現した次世代PET/CT「GEMINI TF」 フィリップスは,商用装置として世界初のTime of Flight(TOF)技術を搭載した次世代PET/CT「GEMINI TF」を開発した(図1)。 |
 図1 GEMINI TF |
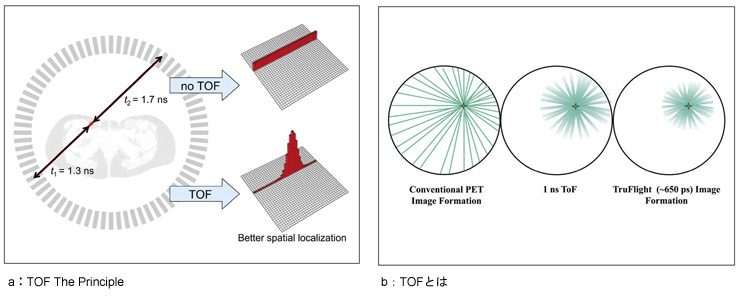 図2 TOF概念図 |
GEMINI TFは,PETにおいて大切な5つのコンポーネント(シンチレータ,検出器,光電子増倍管,電気回路,画像再構成法)を最適化することにより,時間分解能650ps(ピコ秒)を安定して確保することが可能になった(図3)。 SNRincrease=(D/Δx)1/2……式(1) 例えば,腹部径40cmの被検者を時間分解能650psの装置で検査すると,式(1)より,(40cm/10cm)1/2=2となり,2倍のSNRが理論的に得られることになる。 |
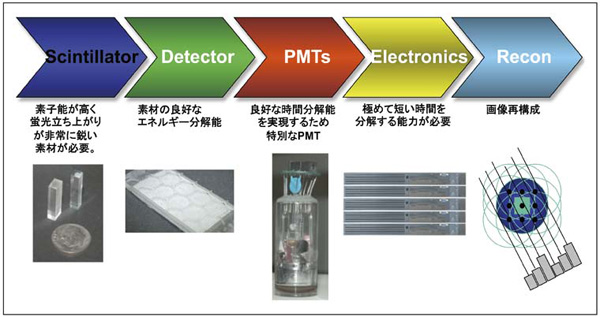 図3 GEMINI TFのハードウエア  図4 TOFの昨今 |
■ TOFを実現する最尤推定法 全身PET検査において腹部領域の検査は,減弱(吸収)によって相対的に信号量が少なくなり,散乱,偶発同時計数の増加によりノイズの増加が著しい部位である。画像再構成上,問題となるのは偽陽性像となる,いわゆる「ホットスポット」像である(図5)。 |
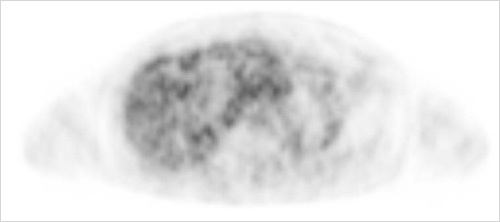 図5 肝臓におけるノイズ これは最尤推定法(統計学的画像再構成法)による計算が収束せず発散してしまった場合に見られ,投与量,収集時間,画像再構成条件などが最適化されていない場合によく見られる画像で,陽性集積との鑑別が必要になる。 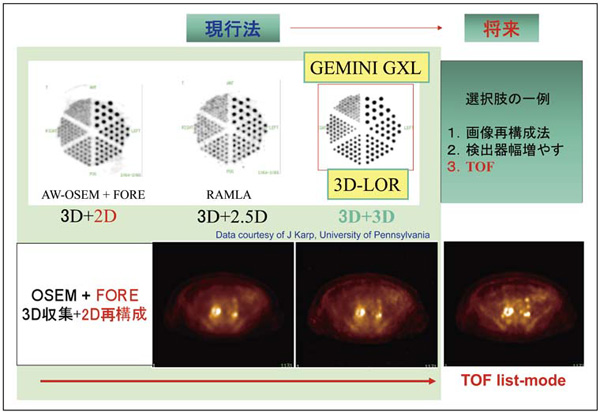 図6 フィリップスPET/CTにおける画像の違い 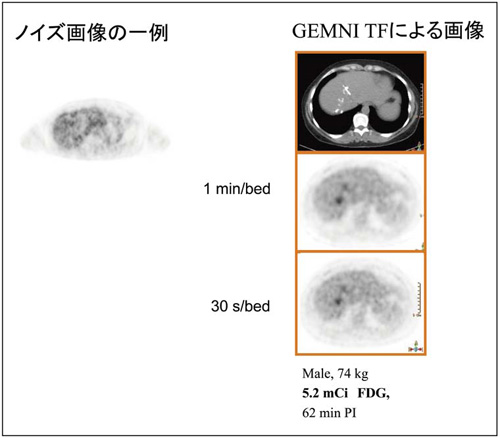 図7 GEMINI TFの画像(Images Courtesy of Saint-Luc Hospital, Brussels) 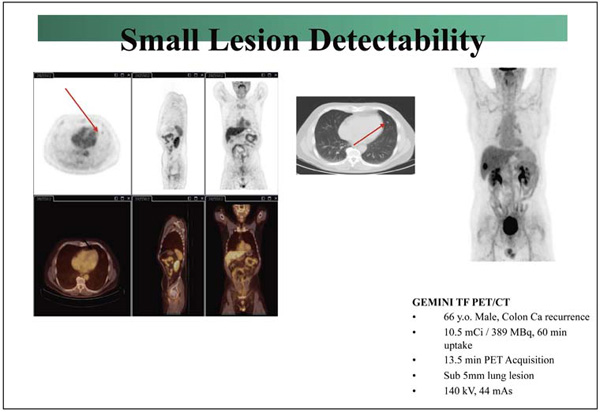 図8 GEMINI TFの画像(Images Courtesy of University Hospitals, Cleveland) |
|
TOF搭載のPET/CT装置は数年後続々と登場してくるであろう。 |
| ●参考文献 | |
| 1) | Budinger, T.F. : Time-of-flight positron emission tomography ; Status relative to conventional PET. J. Nucl. Med., 24・1, 73〜78, 1983. |
| 2) | 尾川浩一 : ECTにおける反復的画像再構成. 日本放射線技術学会雑誌. 56・7, 890〜894, 2000. |
| 3) | Browne, T., et al. : A row-action alternative to the EM algorithm for maximizing likelihoods in emission tomography. IEEE Trans. Med. Imaging, 15・5, 687〜699, 1996. |
| 4) | Kadrmas, D., et al. : LOR-OSEM ; Statistical PET reconstruction from raw line-of-response histograms. Physics in med. & Bio., 49・20, 4731〜4744, 2004. |